Mis sur le marché à la fin des années 80
Une avancée énorme dans le traitement de l’anémie :
- Diminution du nombre de transfusion
- Amélioration la qualité de vie des patients
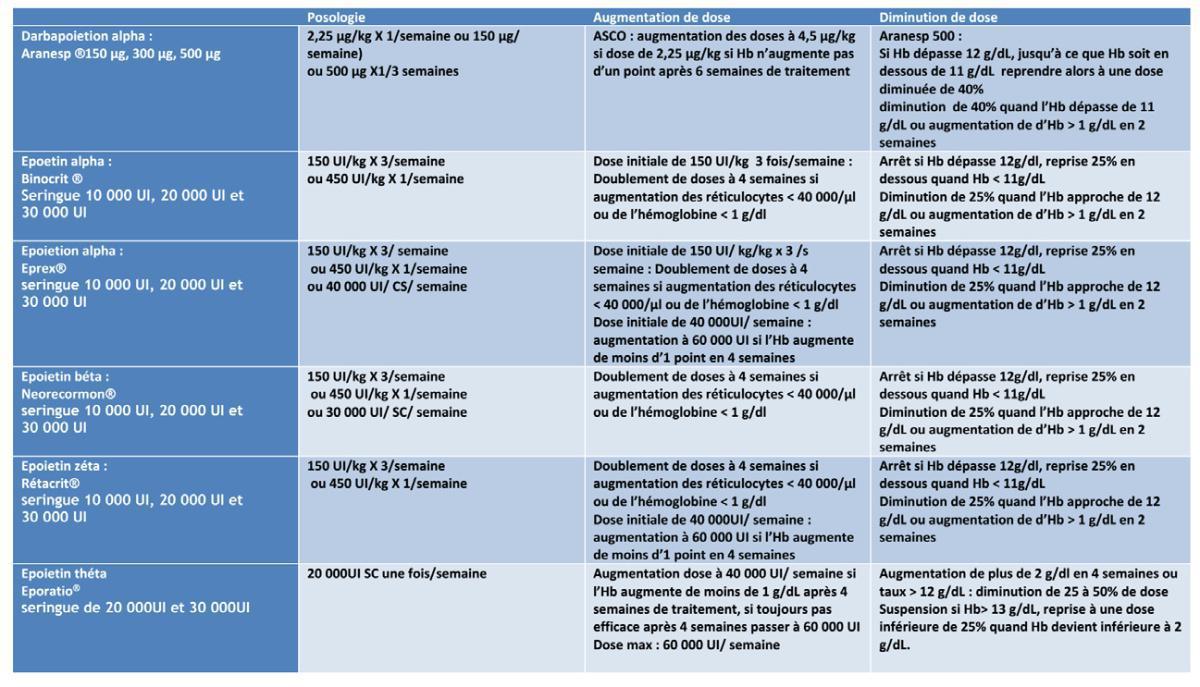
Les différentes Epo disponibles en France avec leur posologie sont résumés dans le tableau présenté en annexe du chapitre (annexe n°2).
Comment prescrire une Epo ?
- Prescription sur ordonnance de médicaments d’exception.
- Ordonnance pour faire pratiquer l’injection à domicile par une infirmière à domicile
Quand prescrire une Epo ?
- L’administration d’EPO doit être proposée de façon individuelle en fonction des données cliniques (âge, état général, retentissement de l’anémie, risque coronarien) et du taux d’hémoglobine.
- Plusieurs recommandations ont été établies ses dernières années et diffèrent quelques peu selon la société savante (ASCO-ASH, EORTC) qui les a établies. La différence essentielle réside sur le taux d’hémoglobine choisi pour initier le traitement.
Management du traitement par EPO
- Réaliser un bilan martial avant de débuter une Epo
- Surveillance régulière de la ferritine et coefficient de saturation (tous les 2 mois), de la NFS
- et des réticulocytes (toutes les 2 à 3 semaines) pendant le traitement
- En cas d’inefficacité au bout de 8 semaines, pas d’intérêt à poursuivre l’EPO
- Poursuivre le traitement 4 semaines après l’arrêt de la chimiothérapie.
- Taux d’Hb cible = 12g/dL.
- Arrêt de l ’Epo lorsque le taux cible est atteint, reprise possible si l’Hb est ≤ 11 g/dL à une dose inférieure de 25% à la précédente.
- Si le taux d’HB augmente de plus de 2 point en 4 semaines ou de plus de 1 point en 2 semaines, les doses devront être adaptées (réduction de 25 à 50%).
Prescription de fer ?
- L’utilisation des Epo peut être responsable d’un déficit fonctionnel en fer : malgré des ré- serves de fer normales, le transport des stocks de fer tissulaire vers la moëlle hématopoïétique est insuffisant. Un déficit fonctionnel en fer peut exister indépendamment de l’utilisation de l’Epo et être dû à la sécrétion de cytokines par les cellules cancéreuses.
- Les études parues récemment sont en faveur de l’utilisation du fer IV (sur la réponse héma- tologique). Cependant, les données sont insuffisantes pour établir des recommandations (posologie ? Fréquence d’administration ? Durée ?).
- Nécessité du suivi de la ferritinémie et du coefficient de saturation de la transferrine pen- dant le traitement par fer IV.
- Pas de supplémentation en fer en cas du surcharge martiale (définie en cancérologie par ferritinémie est > à 1000 et un coefficient de saturation de la transferrine > 45%)
- Arrêt du traitement si ferritine supérieure à 1000 μg/L, reprise possible si de nouveau infé- rieure à 500 μg/L.
| Ferritine < 800 ng/mL et coefficient de saturation transferrine < 20% : discuter fer IV et Epo Ferritine < 30 ng/mL et coefficient de saturation transferrine < 15% : fer IV et Epo |
- Deux types de médicaments disponibles en France :
- hydroxyde ferrique (Ferrograd®, Venofer®) : 100 mg par semaine jusqu’à la sixième semaine, puis 100 mg toutes les deux semaines à partir de la huitième semaine
- carboxymaltose ferrique (Ferinject®). Peu d’études sont disponibles en cancérologie. Le fe- rinect présente l’avantage de pouvoir être utilisé à domicile en une seule injection.
| Taux d’Hb | Patients avec un poids coporel de 35kg à < 70kg | Patients avec un poids corporel ≥ 70 kg |
| < 10 g/dL | 1500 mg | 2500 mg |
| ≥ 10 g/dL | 1000 mg | 2000 mg |
- L’hydroxyde de fer non recommandé à domicile en raison du risque d’allergie.
- AMM pour la carboxymaltose de fer en cas de carence martiale lorsque les formes orales ne sont pas efficaces ou non disponibles.
Quid de la transfusion ? reco ANAES
- Seuils transfusionnels : Hb < 8 g/dL,
- si en cas de signes ou d’antécédents cardio-vasculaires où le seuil transfusionnels : Hb< 10 g/dL.
- Principal intérêt de la transfusion : correction rapide des symptômes.
- Pour une Hb > 8 g/dL, recours à la transfusion seulement si nécessité d’une correction rapide de l’anémie.
Et les bio similaires ?
- Les brevets protégeant les médicaments issus des biotechnologies arrivent à expiration et les fabricants possédant les compétences et les technologies nécessaires pour fabriquer ce type de produits peuvent développer des produits de substitution et en demander l’AMM. ces médicaments de substitution issus des biotechnologies sont appelés bio simi- laires.
Principaux effets secondaires
- Hypertension artérielle, accidents vasculaires cérébraux
- Accidents thromboemboliques
- Céphalées
- Prurit
- Douleur au point de ponction
EPO et survie lors traitement par radio et chimiothérapie
Un effet délétère sur la survie a été rapporté dans quelques études, notamment en association à la radiothérapie. Lorsque les Epo sont utilisées en cas d’anémie chimio induite et en respectant scrupuleusement les recommandations, il n’y pas d’effet délétère sur la survie.
| Radiothérapie et ASE Standard Il n’existe pas d’attitude Standard. Options
|
| Score d’ELYPSE PS > 1 Lymphocytes ≤ 700ul Taux d’Hb < 12 g/dl |
ORGANIGRAMME EPO
PRINCIPALES EPO ET ADAPTATION POSOLOGIQUE
Références bibliographiques :
Aapro M et al., The oncolgist 2008; 13 (suppl 3) : 33-96 Aapro M et al., JCO 2008; 26(4) : 592-8
Aapro M. et al., Br J Cancer 2008; 99 (1) : 14-22 Auerbach M. et al., JCO 2004; 22 (7) : 1301-1307 Auerbach M. et al., JCO 2008; 28 (10) : 1579-1581 Bastit L. et al., JCO 2008; 26 (10) : 1611-1618
Bohlius J. et al., Cochrane Database Syst Rev 2009; 3 : CD007303 Bohlius J. et al.; Lancet 2009; 373 (9674) : 1532-42
Bokemeyer C. et al., Europ J Cancer 2007; 43 (2) : 258-270
Gemic C et al., BMC Cancer. 2016 Aug 20;16(1):661
Grotto HZW et al., Med Oncol 2008; 25 (1) : 12–21
Hedenus M. et al., Leukemia 2007; 21 (4) : 627-632
Henke M. et al., Lancet 2003; 18(11) : 1255-1260
Henry D.H. et al., The Oncologist 2007; 12 (2) : 231–242
Ludwig H. et al., JCO 2009; 27 (17) : 2838-2847
Machtay M. et al., Int J Radial Oncol Biol Phys 2007; 69 (4) : 1008-1017 Marchal C. et al., Cancer/Radiothérapie 2008;12 (2) : 126–133 Mhaskar R et al., Cochrane Database Syst Rev. 2016
Pedrazzoli P. et al., Cancer 2009; 115 (6) : 1169-1173 Pedrazzoli P. et al., JCO 2008; 26 (10) : 1619-1625
Référentiels inter régionaux de soins oncologiques de support, AFSOS décembre 2010 Rizzo JD et al, JCO 2010; 28 (23) : 4996-5010
Steensma DP et al., J Clin Oncol. 2011; 29(1) : 97-105
Tonelli M. et al., CMAJ 2009; 180 (11) : E62-E71A